LONDRES–(BUSINESS WIRE)–Aptorum Group Limited (Nasdaq : APM, Euronext Paris : APM) (« Aptorum Group »), société biopharmaceutique axée sur le développement de nouveaux produits thérapeutiques, incluant le développement d’approches thérapeutiques de nouvelle génération ciblant la résistance antimicrobienne, a annoncé deux séries de résultats positifs montrant à la fois une importante activité in vivo de son composé majeur ALS-4 contre le staphylocoque doré résistant à la méticilline (SDMR, l’une des “superbactéries”) respectivement dans des modèles souris de plaies infectées et de bactériémie en comparaison des antibiotiques actuels.
ALS-4 est actuellement en phase finale des études permettant le dépôt d’une demande d’homologation comme NMR (nouveau médicament de recherche), qui implique un contrôle de la toxicité orale de 14 jours sur des rats et des chiens, une série d’observations fonctionnelles sur des rats et une étude sur la santé respiratoire et de télémétrie cardiovasculaire sur des chiens. Sous réserve des résultats définitifs des études permettant le dépôt d’une demande d’homologation comme NDR, ALS-4 devrait faire l’objet d’un dépôt réglementaire au T4 2020, qui déterminera le commencement des essais cliniques de Phase I au Canada.
« En dépit des deux traitements de base actuels, la vancomycine et la daptomycine, qui sont les seuls antibiotiques approuvés à ce jour par la FDA pour traiter la bactériémie à SDMR, les taux de mortalité, de morbidité et de récidive restent importants1. Le flux d’antibiotiques à venir étant fragile et à risque à l’échelle mondiale, les problèmes de résistance antimicrobienne continuent de retenir toute l’attention des organisations internationales comme l’Organisation mondiale de la santé et la FDA, ainsi que de l’industrie pharmaceutique. Nous pensons que notre médicament oral ALS-4, basé sur une nouvelle approche de l’anti-virulence, peut potentiellement lutter contre tout un éventail d’infections liées au SDMR, y compris (mais sans s’y limiter) la bactériémie et les infections de la peau et des tissus mous, sous réserve de l’issue positive des essais cliniques respectifs. Nous sommes particulièrement encouragés par les résultats car ALS-4 semble être efficace contre la superbactérie SDMR et pourrait constituer un potentiel traitement alternatif et durable pour différentes indications de SDMR dont, entre autres, la bactériémie à SDMR et les infections cutanées. Les propriétés d’anti-virulence d’ALS-4 représentent une approche nouvelle pour aborder les problèmes de résistance antimicrobienne, encouragée par les récents plans d’action globaux. Nous sommes également ravis d’annoncer que nos études permettant le dépôt d’une demande d’homologation comme NMR sont aussi à leurs derniers stades, et nous respectons I ’échéancier pour effectuer le dépôt réglementaire qui déterminera le commencement des essais cliniques de Phase 1 », a affirmé M. Darren Lui, Président et Directeur exécutif de la société.
Efficacité d’ALS-4 dans un modèle murin d’infection des plaies par le SDMR
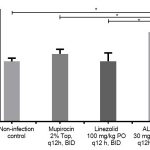
Une étude récente, menée par un organisme de recherche contractuelle tiers, a évalué l’impact d’ALS-4 sur la cicatrisation de plaies ouvertes infectées par le SDMR dans un modèle murin. Par rapport à une posologie topique de 2 % de mupirocine et à une posologie orale de linézolide selon une administration de 100 mg/kg deux fois par jour, la posologie orale d’ALS-4 à 30 mg/kg deux fois par jour a affiché une amélioration statistiquement significative de la cicatrisation des plaies. En particulier, à la fin de l’étude, au 7e jour, ALS-4 a permis une fermeture des plaies de 63,8 %, contre 48,4 % pour le linézolide par voie orale et 43,2 % pour le mupirocine à 2 % par voie topique. Les résultats sont illustrés plus en détail dans le graphique ci-dessus.
Efficacité d’ALS-4 dans un modèle murin de bactériémie
Dans le cadre d’une autre série d’études in vivo menées par un organisme de recherche contractuelle tiers, sur un modèle murin de bactériémie à SDMR non létale, les souris ont reçu par voie orale différentes doses d’ALS-4 allant de 0,3 à 30 mg/kg deux fois par jour pendant 7 jours, alors que d’autres faisaient partie d’un groupe recevant uniquement de la vancomycine (3 mg/kg de vancomycine administré par voie intraveineuse) ou d’un groupe témoin ne recevant aucun traitement.
À la fin de l’étude le septième jour, ALS-4 a permis une réduction statistiquement significative de la numération bactérienne dans les principaux organes comme les reins, les poumons, le foie et la rate par rapport au groupe témoin ne recevant aucun traitement et au groupe recevant uniquement de la vancomycine (test t des étudiants non apparié, p<0,05). Cela s’ajoute aux précédents résultats d’études in vivo annoncés en février 2020, ayant démontré qu’ALS-4 offrait, sur une base statistiquement significative, de meilleurs taux de survie (56 % contre 0 % pour le groupe témoin) dans le modèle rat de bactériémie à SDMR létale et une réduction plus importante de la charge bactérienne (de 99,5 % par rapport au groupe témoin) dans le modèle rat de bactériémie à SDMR non létale.
À propos de la molécule ALS-4
Faisant partie de la plateforme pour les maladies infectieuses Acticule d’Aptorum Group, ALS-4 est une nouvelle petite molécule, première de sa classe, développée sous forme orale et basée sur une approche de l’anti-virulence ciblant le staphylocoque doré résistant à la méticilline (SDMR). ALS-4 cible les propriétés de résistance antimicrobienne du staphylocoque doré et permet aux bactéries de devenir très sensibles à la clairance immunitaire de l’hôte et aussi potentiellement à d’autres antibiotiques existants, comme le montrent les données précliniques.
À propos d’Aptorum Group Limited
Aptorum Group Limited (Nasdaq : APM, Euronext Paris : APM) est une société pharmaceutique dédiée au développement et à la commercialisation de nouveaux produits thérapeutiques destinés à répondre à des besoins médicaux non satisfaits. Aptorum Group poursuit des projets thérapeutiques dans les domaines des maladies orphelines, des maladies infectieuses, des maladies métaboliques, de la santé des femmes et dans d’autres domaines thérapeutiques.
Pour de plus amples informations au sujet d’Aptorum Group, veuillez consulter www.aptorumgroup.com.
Pour une présentation générale plus large, veuillez visiter : https://ir.aptorumgroup.com/static-files/ca36cc65-6f23-4105-895e-f5f234ecca1e
Clause de non-responsabilité et déclarations prospectives
Le présent communiqué de presse ne constitue pas une offre de vente ni une sollicitation d’offres d’achat de titres d’Aptorum Group.
Le présent communiqué de presse comprend des énoncés relatifs à Aptorum Group Limited et à ses attentes, perspectives et projets futurs, qui constituent des “énoncés prospectifs” au sens de la loi Private Securities Litigation Reform Act de 1995. À cet égard, les énoncés contenus dans ce communiqué qui ne sont pas des énoncés de faits historiques peuvent être considérés comme des énoncés prospectifs. Dans certains cas, vous pouvez identifier les énoncés prospectifs par l’emploi de termes comme “pourrait”, “devrait”, “s’attend à”, “prévoit”, “anticipe”, “a l’intention de”, “cible”, “projette”, “envisage”, “pense”, “estime”, “prédit”, “potentiel” ou “continue”, ou la forme négative de ces termes ou d’autres expressions similaires. Aptorum Group a essentiellement basé ces énoncés prospectifs, qui incluent des déclarations relatives à des échéances prévues pour la soumission de demandes et les essais, sur ses attentes et projections actuelles par rapport aux tendances et événements futurs qui, selon la société, sont susceptibles d’exercer un impact sur son activité, sa situation financière et les résultats de ses opérations. Ces énoncés prospectifs ne sont valables qu’à la date du présent communiqué de presse et sont soumis à un certain nombre de risques, d’incertitudes et d’hypothèses incluant, mais sans s’y limiter, les risques liés aux changements annoncés aux niveaux de la direction et de l’organisation, la rétention et la disponibilité du personnel clé, la capacité de la société à étendre ses gammes de produits en proposant des produits supplémentaires dans d’autres segments de consommation, les résultats de ses activités de développement, les stratégies de croissance prévues de la société, les tendances et difficultés prévues dans ses activités, ses attentes vis-à-vis de sa chaîne d’approvisionnement et la stabilité de celle-ci, les risques détaillés sur le Formulaire 20-F d’Aptorum Group et dans d’autres documents que la Société est susceptible de déposer à l’avenir auprès de la SEC, ainsi que dans le prospectus reçu par l’Autorité des marchés financiers en France (visa n°20-352) le 16 juillet 2020.
En conséquence, les prévisions figurant dans de tels énoncés prospectifs sont susceptibles de changer et les résultats réels pourraient être sensiblement différentes de ceux décrits dans les présentes. Aptorum Group n’assume aucune obligation de mettre à jour les énoncés prospectifs contenus dans ce communiqué de presse à la lumière de nouvelles informations, d’événements futurs ou autre.
Cette annonce n’est pas un prospectus au sens du règlement (UE) n°2017/1129 du 14 juin 2017, tel que modifié par les règlements délégués (UE) n°2019/980 du 14 mars 2019 et n°2019/979 du 14 mars 2019.
Le présent communiqué de presse est fourni “en l’état”, sans représentation ou garantie de quelque nature que ce soit.
________________________________________
1 https://link.springer.com/article/10.1186/s13054-017-1801-3
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Contacts
Aptorum Group limited
Investor Relations Department:
Tel: +852 3953 7700
Email: investor.relations@aptorumgroup.com
Actifin – Financial Communications Europe
Investor relations
Ghislaine Gasparetto
ggasparetto@actifin.fr
+33 1 56 88 11 22
Redchip – Financial Communications United States
Investor relations
RedChip Companies, Inc.
dave@redchip.com
+1 407 491 4498